
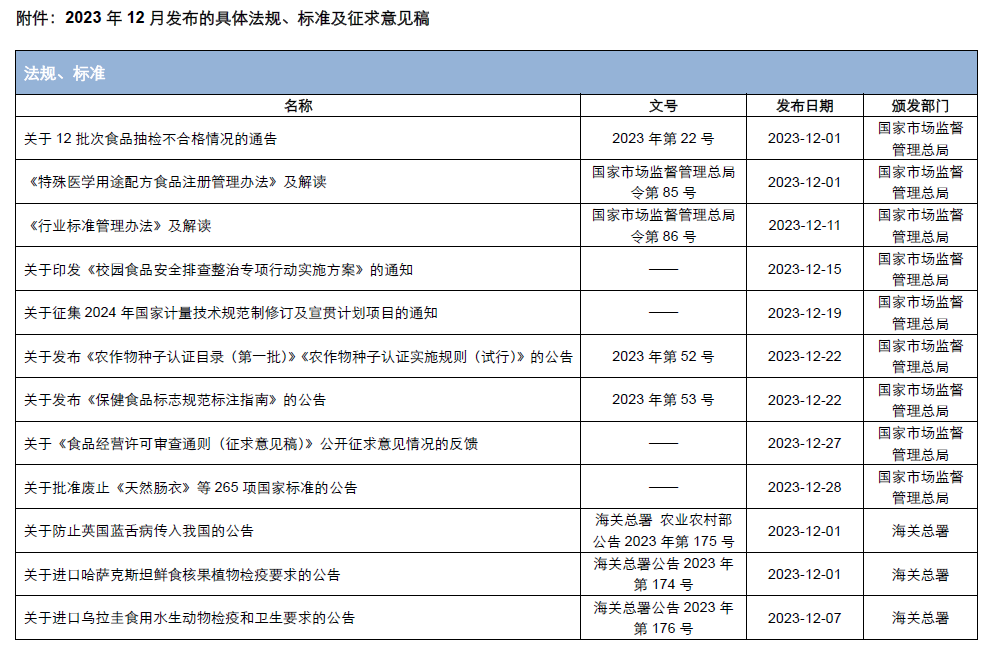
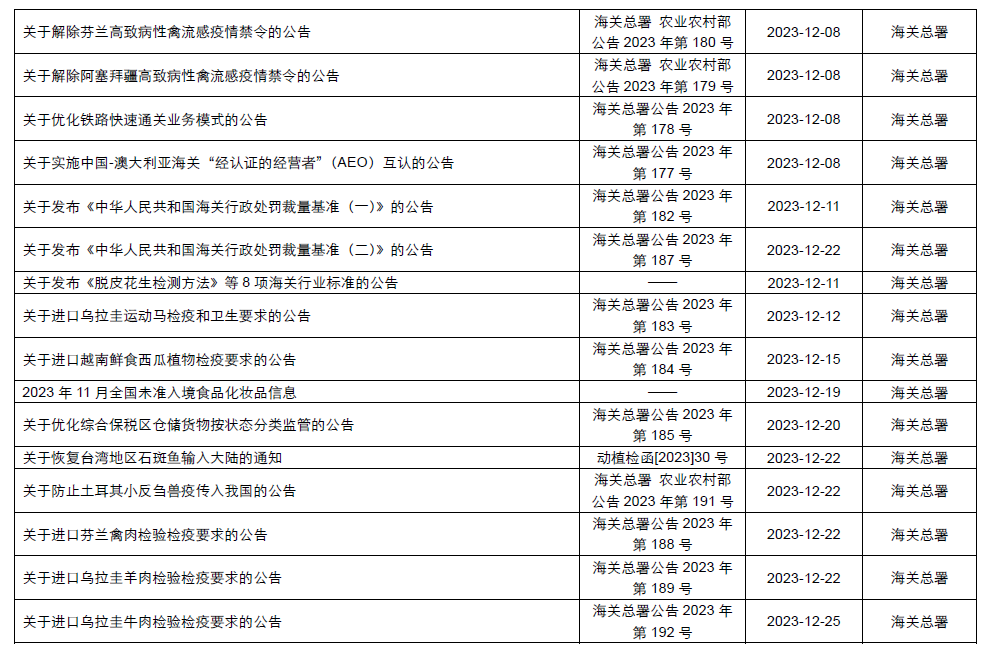
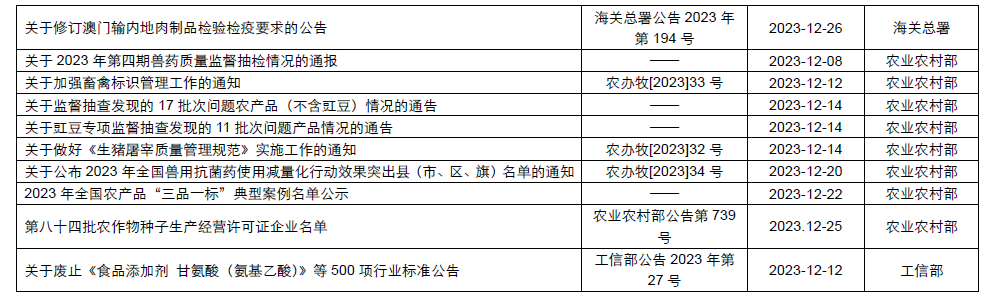
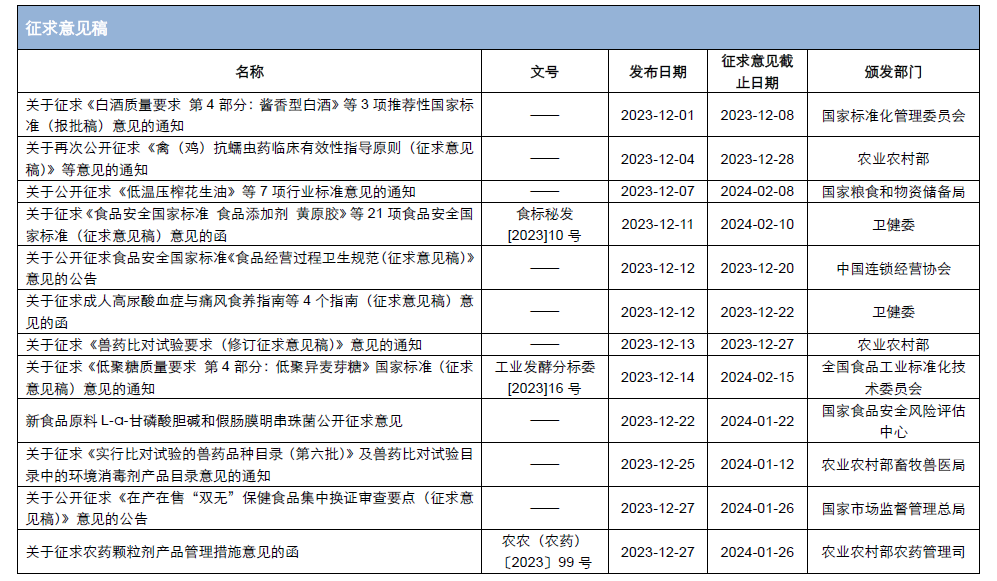
本月,各政府監管機構陸續發布了一(yī)些食品相關的重要法規标準、征求意見稿及公告。其中(zhōng),國家衛生(shēng)健康委員(yuán)會發布了關于征求《食品安全國家标準 食品添加劑 黃原膠》等21項食品安全國家标準(征求意見稿)意見的函;市場監管總局發布了《特殊醫學用途配方食品注冊管理辦法》及解讀、《行業标準管理辦法》及解讀、《保健食品标志(zhì)規範标注指南(nán)》、關于公開(kāi)征求《在産在售“雙無”保健食品集中(zhōng)換證審查要點(征求意見稿)》意見的公告;國家食品安全風險評估中(zhōng)心就新食品原料L-α-甘磷酸膽堿和假腸膜明串珠菌公開(kāi)征求意見。
爲了更好地幫助企業落地法規,北京睿伯乐企业管理咨询有限公司對2023年12月份發布的重點法規、标準以及征求意見稿進行了簡單解讀,同時對本月發布的食品相關法規标準等進行了彙總,供大(dà)家參考。
一(yī)、多項食品安全國家标準公開(kāi)征求意見
2023年12月11日,《食品安全國家标準 食品添加劑 黃原膠》等21項食品安全國家标準(征求意見稿)的标準修改單公開(kāi)征求意見,包括食品添加劑1項:修訂《食品添加劑 黃原膠》;生(shēng)産經營規範3項:修訂《食品生(shēng)産通用衛生(shēng)規範》、《保健食品良好生(shēng)産規範》;食品相關産品1項:修訂《食品接觸用塗料及塗層》;食品産品3項:修訂《巴氏殺菌乳》、《滅菌乳》,制定《高溫殺菌乳》。反饋截止日期爲2024年2月10日。
2023年12月1日,市場監管總局發布了《特殊醫學用途配方食品注冊管理辦法》與解讀文件,包括總則、申請與注冊、臨床試驗、标簽和說明書(shū)、監督檢查/監督管理、法律責任、附則七章共六十四條内容。此次修訂與舊(jiù)版相比,嚴格了注冊要求,明确不予注冊情形;新增優先審評審批程序鼓勵企業研發注冊臨床急需、罕見病類别等特殊醫學用途配方食品,以滿足臨床需要,并設置了相應優先審評審批程序,明确适用範圍及政策支持措施。納入優先審評審批程序的産品,審評時限爲從六十個工(gōng)作日壓縮爲三十個工(gōng)作日。《辦法》于2024年1月1日起施行,2016年3月7日原國家食品藥品監督管理總局令第24号公布的《特殊醫學用途配方食品注冊管理辦法》同時廢止。
三、保健食品标志(zhì)規範标注指南(nán)發布以及《在産在售“雙無”保健食品集中(zhōng)換證審查要點(征求意見稿)》公開(kāi)征求意見
2023年12月12日市場監管總局發布《保健食品标志(zhì)規範标注指南(nán)》(以下(xià)簡稱《指南(nán)》),指導保健食品生(shēng)産經營者進一(yī)步規範标注保健食品标志(zhì)。《指南(nán)》中(zhōng)保健食品專有标志(zhì)圖形、顔色與原規定原則保持一(yī)緻,明确了保健食品标志(zhì)框架、圖形比例等内容。保健食品生(shēng)産經營者應切實履行食品安全主體(tǐ)責任,按照《指南(nán)》規範标注保健食品标志(zhì),可在生(shēng)産經營場所、專區專櫃、廣告中(zhōng)使用保健食品标志(zhì);可按照法律法規規定,結合自身實際在保健食品産品運輸箱、中(zhōng)轉箱等包裝材料上規範使用保健食品标志(zhì)。
2023年12月27日,爲規範原衛生(shēng)部等過去(qù)不同時期批準的“無有效期、無産品技術要求”(以下(xià)簡稱“雙無”)保健食品注冊證書(shū),完善注冊信息,統一(yī)監管标準,市場監管總局經廣泛征求意見,制定本審查要點。規定在過渡期内,省級市場監管部門繼續按照現行規定發放(fàng)生(shēng)産許可,持有效生(shēng)産許可的“雙無”産品集中(zhōng)換證,由生(shēng)産許可核發地省級市場監管部門出具換證意見。《要點》同時說明了詳細的換證程序以及具體(tǐ)要求,意見建議反饋截止時間爲2024年1月26日。
四、2種新食品原料公開(kāi)征求意見,甜葉菊等3種新食品原料終止審查
2023年12月22日,新食品原料L-α-甘磷酸膽堿和假腸膜明串珠菌已通過專家評審委員(yuán)會技術審查,現公開(kāi)征求意見,反饋截止時間爲2024年1月22日。
L-α-甘磷酸膽堿推薦食用量≤600毫克/天,嬰幼兒、孕婦和哺乳期婦女不宜食用,标簽、說明書(shū)應當标注不适宜人群和食用限量,随公告附有其質量規格和食品安全指标;
假腸膜明串珠菌批準列入《可用于食品的菌種名單》,使用範圍包括發酵乳、風味發酵乳、幹酪、發酵型含乳飲料、乳酸菌飲料(非固體(tǐ)飲料)、稀奶油、奶油(黃油)和無水奶油(無水黃油),不包括嬰幼兒食品。
同時,新食品原料終止審查目錄也發生(shēng)變化,甜葉菊、兩色金雞菊、金花茶花朵3種新食品原料終止審查。
甜葉菊的申報于2023年7月19日受理,受理編号爲衛食新申字(2023)第0008号,由于其在我(wǒ)國多省具有長期人群食用曆史,建議終止審查,食品安全指标按照我(wǒ)國現行食品安全國家标準中(zhōng)葉菜蔬菜的規定執行。
北京睿伯乐企业管理咨询有限公司希望通過對十二月法規回顧以及重點法規的解讀,對企業及行業人員(yuán)把握監管變化趨勢、合規宣傳産品有所幫助。北京睿伯乐企业管理咨询有限公司可提供标準法規咨詢、行業輿情監控、食品标簽審核等咨詢服務,有任何問題歡迎随時聯系我(wǒ)們(010-51301566)。
 京公網安備11010502045875
京公網安備11010502045875